Artigo comentado
Bell KJ, Fio CZ, Twigg S, et al. Amount and Type of Dietary Fat, Postprandial Glycemia, and Insulin Requirements in Type 1 Diabetes: A Randomized Within-Subject Trial. Diabetes Care 2020;43:59–66.
O impacto da gordura e proteína da dieta sobre a glicemia pós-prandial em Diabetes tipo 1 (DM1) e a necessidade de ajustes na dose de insulina das refeições tem sido controverso. Recentemente ensaios clínicos randomizados em indivíduos com DM1 mostraram que a proteína e a gordura consumida em refeições com carboidratos reduzem o aumento glicêmico pós-prandial precoce (1–2 h) e contribui para a hiperglicemia pós-prandial tardia (3-6 h). Na prática clínica, o monitoramento contínuo da glicose destaca os efeitos glicêmicos de diferentes tipos de refeições demonstrando que estratégias de dosagem de insulina das refeições baseadas somente em contagem de carboidratos têm limitações. Desde 2017, a American Diabetes Association recomenda que pessoas com Diabetes tipo 1 considerem as proteínas e gorduras da refeição, além da contagem de carboidratos, para ajustes das doses de insulinas prandiais, a fim de melhorar o controle glicêmico pós prandial. Porém, conforme discutido amplamente em publicação da Nota Técnica da Sociedade Brasileira de Diabetes (SBD) em 2019, sobre Conversão de ingestão de proteínas e gorduras para bolus alimentar, não há até o momento um algoritmo único e seguro para consideração desses macronutrientes na dose de insulina. Ainda se faz necessário desenvolvimento de método prático e seguro, baseado em evidências, para orientar os ajustes de insulina para refeições com alto teor de gorduras e proteínas.
A Nota técnica da SBD cita e se baseia principalmente em um artigo de revisão sistemática com análise de vários estudos bem conduzidos nessa área e é sugerido como um dos algoritmos, um adicional de em média 30-35% da dose de insulina calculada pela contagem de carboidratos para a consideração de refeições que tenham maior quantidade de proteínas e gorduras. A grande preocupação é que o adicional dessa dose, se aplicada previamente ou no momento da refeição, há maior risco de hipoglicemia precoce (até 120 min após a refeição), pois o esvaziamento gástrico de refeições com essa natureza é mais lento, além de esses macronutrientes terem efeito de conversão de glicose mais tardiamente. Essa adição é sugerida em torno de 1 hora após a refeição quando em terapia de múltiplas doses de insulina, e em bomba de insulina, em bolus duplo dividindo dose total calculada em infusão de 50% da dose imediatamente antes da refeição e os outros 50% em bolus estendido em 2h a 2h30min. A utilização desses ajustes para usuários de bomba de insulina se faz de forma mais segura em relação ao risco de hipoglicemias, mas é sabida a dificuldade de acesso à essa terapia, não sendo a realidade da maioria dos pacientes com DM1 no Brasil. Além disso, foi demonstrado que os efeitos da ingestão de proteínas e gorduras na glicemia é variável em cada indivíduo, com alguns pacientes não precisando de adicional de insulina para alguns teores de proteínas e gorduras e outros precisando de até o dobro da dose, o que torna a questão ainda mais cautelosa e com a necessidade de ajustes individualizados.
Dentro desse panorama, o grupo de Kirstine Bell e colaboradores, autora da revisão sistemática publicada em 2015, citada anteriormente, abordam a questão clínica como urgente, visto que a hiperglicemia pós-prandial foi identificada como fator de risco para o desenvolvimento de complicações de longo prazo do diabetes, e dietas com alto teor de gordura aumentaram em popularidade nos últimos anos. Recentemente, o grupo de Bell publicou na Diabetes Care em 2020, estudo randomizado, dentro do assunto para examinar as necessidades de insulina para doses incrementais de gordura. Este estudo teve como objetivo determinar 1) a relação entre a quantidade e o tipo de gordura dietética e a glicemia e 2) os ajustes ideais de insulina para gordura dietética.
Adultos com DM1 usando terapia com bomba de insulina compareceram à clínica de pesquisa em 9 a 12 ocasiões. Nas primeiras seis visitas, os participantes consumiram refeições contendo 45 g carboidrato com 0 g, 20 g, 40 g ou 60 g de gorduras, variando em fontes de gordura saturada, monoinsaturada ou poliinsaturada. A insulina foi dosada pela proporção insulina / carboidrato (ICR) individual administrada em onda dupla 50/50% ao longo de 2 h. Nas visitas subsequentes, os participantes repetiram as refeições de 20-60 g de gordura com a dose de insulina estimada usando um modelo preditivo de bolus (MPB), até duas vezes por refeição, até que o controle glicêmico fosse alcançado.
Com a mesma dose de insulina, o aumento da quantidade de gordura resultou em uma significativa redução na área incremental sob a curva para glicose no período pós-prandial inicial (0–2 h; P = 0,008) e aumento no período pós-prandial tardio (2–5 h; P = 0,004). O tipo de gordura não fez diferença significativa na curva glicêmica nas 5 horas analisadas após as refeições. Para alcançar o controle glicêmico, em média os participantes necessitaram de bolus de insulina de onda dupla: para 20 g de gordura, + 6% de insulina, 74/26% em 73 min; 40 g de gordura, + 6% de insulina, 63/37% em média 75 min; e 60 g de gordura, + 21% de insulina, 49/51% em 105 min.
A principal descoberta foi que a média de insulina adicional necessária aumentou 6% para uma refeição de 20 g e 40 g de gorduras extras, e 21% para mais 60 g de gordura. A variação interindividual foi alta, apoiando achados de estudos anteriores, com metade dos participantes que consumiram a refeição com 40 g de adição de gordura exigindo apenas a dose usual. O algoritmo de um modelo de controle preditivo promete, pois melhora a área sob a curva de glicose após refeições com alto teor de gordura, sem aumento na hipoglicemia. No entanto, as diferenças interindividuais destacam os desafios na tradução clínica e recomendações. Algoritmos alternativos para conversão de proteínas e gorduras são mais complexos do que aqueles apenas para carboidratos. Fatores adicionais precisam ser considerados no cálculo da insulina para gordura e proteína. Em refeições mistas, um ajuste na proporção de insulina para carboidrato é necessário devido às interações entre carboidratos, gorduras e proteínas na resistência à insulina. Quando proteínas ou gorduras são consumidas sozinhas ou como parte de uma refeição mista, fatores independentes, proporcionais à quantidade de gordura e proteína, são necessários considerar por mecanismos como a gliconeogênese.
Bell e colaboradores adicionaram a essas descobertas por demonstrar uma resposta à dose de gordura em uma refeição contendo carboidratos, mostrando reduções dependentes da dose no início do período pós-prandial seguido de aumentos no período pós-prandial tardio.
A fim de fornecer orientação clínica para ajustes de insulina, é necessário primeiro considerar o seguinte: Qual é o impacto de quantidades variáveis de gordura e proteína na glicemia pós-prandial para tal indivíduo? O nutricionista ou médico educador em diabetes deve junto com seu paciente estabelecer o algoritmo que melhor o atenda estudando seu controle glicêmico, tipo de tratamento e disponibilidade do mesmo de forma individual.
Figura 1 – Perfis de glicose pós-prandial para vários tipos (A) (n = 16) e quantidades (B) (n = 15) de gorduras em adultos com DM1 usando terapia com bomba de insulina com insulina dosada de acordo com ICR como onda dupla 50/50% ao longo de 2 h.
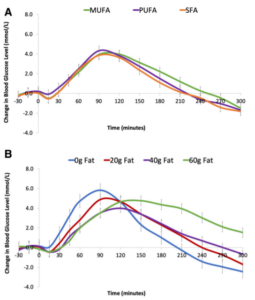
(MUFA – gordura monoinsaturada, PUFA – gordura poliinsaturada, SFA – gordura saturada).
Figura 2 – Perfis de glicose pós-prandial para 20 g (A), 40 g (B) e 60 g (C) de gordura com 45g de carboidrato em 12 adultos com DM1 usando terapia com bomba de insulina quando o bolus de insulina foi dosado de acordo com sua ICR individualizado ou com MPB (modelo preditivo de bolus).
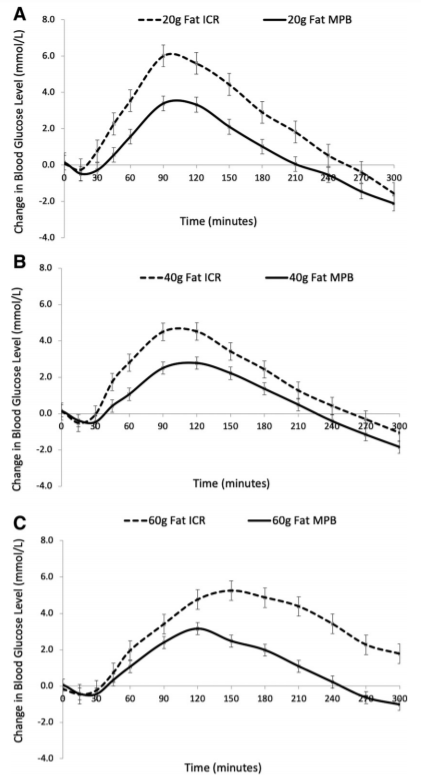
Referências Bibliográficas
Bell KJ, Fio CZ, Twigg S, et al. Amount and Type of Dietary Fat, Postprandial Glycemia, and Insulin Requirements in Type 1 Diabetes: A Randomized Within-Subject Trial. Diabetes Care 2020;43:59–66.
Smart CEM, King BR, Lopez PE. Commentary: Insulin Dosing for Fat and Protein: Is it Time? Diabetes Care 2020;43:13–15.
Bell, K. J. et al. Impact of fat, protein, and glycemic index on postprandial glucose control in type 1diabetes: Implications for intensive diabetes management in the continuous glucose monitoring era. Diabetes Care, 2015.
Nota Técnica da SBD 2019 – Sociedade Brasileira de Diabetes. Terapêutica Nutricional no Diabetes – Conversão de ingestão de proteínas e gorduras para bolus alimentar – Departamento de Nutrição da SBD – Gestão 2018-2019.
- Nutricionista especialista em Nutrição Clínica pelo Ganep
- Mestre em Educação em Diabetes pelo IEP - Santa Casa de Belo Horizonte
- Membro do Departamento de Nutrição da Sociedade Brasileira de Diabetes
- Nutricionista da equipe do Ambulatório de Diabetes tipo 1 da Santa Casa de BH
- Educadora em Diabetes especializada em terapia de bomba de infusão contínua de insulina

